6 hónapos hatása. kalóriakorlátozás a hosszú élettartam, az anyagcsere-adaptáció és az oxidatív stressz biomarkerein túlsúlyos személyeknél
Leonie K Heilbronn
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
2 Garvani Orvosi Kutató Intézet, Darlinghurst, NSW, AUSZTRÁLIA, 2010
Lilian de Jonge
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Madlyn I Frisard
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
James P. DeLany
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
D. Enette Larson Meyer
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Jennifer Rood
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Tuong Nguyen
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Corby K Martin
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Julia Volaufova
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Marlene M Most
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Frank L Greenway
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Steven R Smith
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Donald A Williamson
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Walter A Deutsch
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Eric Ravussin
1 Pennington Biomedical Research Center, Baton Rouge, LA, 70808
Absztrakt
Kontextus
A hosszan tartó kalória-korlátozás (CR) növeli a rágcsálók élettartamát. Azt, hogy a hosszan tartó CR befolyásolja-e a hosszú élettartam biomarkereit, az oxidatív stressz markereit, és csökkenti-e az anyagcserét, meghaladva a csökkent anyagcsere tömegét, még nem vizsgálták emberen.
Célkitűzések
A 6 hónapos kalória-korlátozás hatásainak vizsgálata testmozgással vagy anélkül nonobese-ben (25≤BMI 0,05), de csökkent a CR-ben (-135 (42) kcal/d), CREX (-117 (52) kcal/d) és LCD (-125 (35) kcal/d, (minden, p Kulcsszavak: öregedés, anyagcsere arány, oxidatív károsodás, kalória-korlátozás, maghőmérséklet, inzulin
Bevezetés
A hosszan tartó kalória-korlátozás (CR) növeli a rágcsálók és más rövidebb életű fajok élettartamát 1. Hogy ez hosszabb életű fajokban fordul-e elő, nem ismert, bár a hosszan tartó CR hatását nem főemlősökön vizsgálják. Az egyik hipotézis a CR öregedésgátló hatásainak magyarázatára a csökkent energiafogyasztás (EE), ennek következtében csökken a reaktív oxigénfajok (ROS) termelése 2, 3. A CR-hez kapcsolódó egyéb metabolikus hatások, beleértve a megváltozott inzulinérzékenységet és jelátvitelt, megváltozott neuroendokrin funkciót, megváltozott stresszreakciót vagy ezek kombinációját, késleltethetik az öregedést 4 .
Az összes EE nyugvó EE (az energia 50-80% -a), az etetés hőhatása
10%), és nem pihent EE (10-40%) 5. Arról vitázunk, hogy az energiafelhasználás csökken-e a CR után az metabolizáló tömeg nagyságának adott csökkenésénél várható szint felett. Leibel és mtsai. A 6. ábra azt mutatta, hogy a 10% -os súlyvesztés csökkentette az ülő 24 órás energiafogyasztást a testsúly fenntartása érdekében 15-20% között elhízott egyéneknél, ami arra utal, hogy az embereknél metabolikus alkalmazkodás következik be. A fogyást azonban folyékony étrenddel sikerült gyorsan elérni, és abban a tanulmányban néhány normál testsúlyú alany kivételével a hosszan tartó CR hatása az elhízott emberek energiafogyasztására még nem tesztelt. Rhesus majmokban a pihenő EE zsírmentes tömegre és zsírtömegre igazítva alacsonyabb volt 11 éves CR 7 után. Hasonlóképpen, az összes EE alacsonyabb volt a CR majmokban 10 év súlybefogást követően 8. A rágcsálókon végzett vizsgálatok ellentmondásosabbnak bizonyultak a CR és az ad libitum táplált állatok közötti csökkent, nem változott vagy megnövekedett EE arányának beszámolásával 9 - 13 .
Az öregedés egyik legelterjedtebb elmélete az oxidatív stressz elmélete, amely kimondja, hogy az ROS által okozott oxidatív károsodás idővel felhalmozódik, ami olyan betegségek kialakulásához vezet, mint a rák, az öregedés és végül a halál. A ROS az energia-anyagcsere mellékterméke, az oxigénfogyasztás 0,2-2,0% -a eredményezi a ROS képződését 15, 16. A ROS megtámadja a lipideket, fehérjéket és DNS-t, és számos olyan terméket állít elő, amelyek befolyásolják a sejtek normális működését 17. Rágcsálókon végzett vizsgálatok azt mutatják, hogy az agyban, a vázizomban és a szívben a 8-oxo7,8-dihidro2'-deoxiguanozin (8oxodG) 30% -kal csökken, az agy és az izmok 18-22-ben a karbonil-tartalom hasonló csökkenést mutat, és transzkripciós mintákat mutatnak, amelyek csökkent oxidatív stresszre utalnak válaszul a CR 23-ra. A kalória-korlátozásnak alávetett rhesusmajmok azonban eltérő válaszokat mutatnak az oxidatív stresszben érintett gének expressziójában 24 .
A maghőmérséklet, a dehidroepiandroszteron-szulfát (DHEAS) és az inzulin a CR és a hosszú élettartam javasolt biomarkerei rágcsálókban és majmokban 25. Az idősödés Baltimore longitudinális vizsgálatának adatai alátámasztják a hosszú élettartam és a hőmérséklet, az inzulin és a DHEAS összefüggését azoknál a férfiaknál, akiknél a plazma inzulin koncentrációja vagy orális hőmérséklete medián alatt van, és a DHEAS meghaladja a medián hosszabb életet 26. Továbbá egy keresztmetszeti vizsgálatban, amely összehasonlította az 6 éven át önállóan táplálkozásilag megfelelő CR-vel rendelkező embereket a normál testsúlykontrollal, Fontana és mtsai 27. arról számoltak be, hogy a CR alanyoknak alacsonyabb volt a szérum glükóz, inzulin és az ateroszklerózis markerei.
A tanulmány célja annak meghatározása volt, hogy az elhúzódó CR diétával önmagában vagy a testmozgással együtt sikeresen megvalósítható-e nem elhízott személyeknél, valamint hogy meghatározzuk a beavatkozások hatásait a CR kimutatott biomarkereire, a mozgásszegény energiafelhasználásra és a DNS oxidatív károsodására és fehérjék.
Mód
Az energiafogyasztás csökkentésének hosszú távú hatásainak átfogó értékelése (CALERIE) egy randomizált klinikai vizsgálat, amelyet az Országos Öregedési Intézet finanszírozott a Louisiana államban, a Pennington Biomedical Research Center-ben. A Penningtoni Belső Ellenőrző Testület és egy független adatbiztonsági ellenőrző testület jóváhagyta a protokollt, és az alanyok írásbeli, tájékozott beleegyezést nyújtottak be. A tanulmány 2002. augusztusa és 2004. júliusa között készült.
Tárgyak
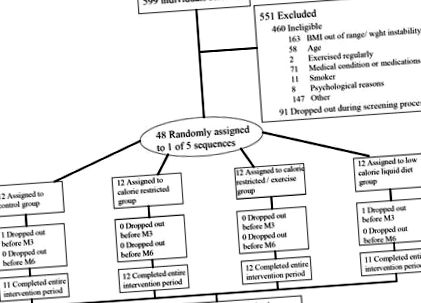
A potenciális résztvevők 3 szűrővizsgálatot tettek meg, amelyek során számos paramétert rögzítettek annak biztosítására, hogy az alanyok fizikailag és pszichológiailag egészségesek legyenek, beleértve a testmagasságot, a súlyt, a vérnyomást, az elektrokardiogramot, a kémia 15 paneljét és a teljes vérképet. Ötszázkilencvenkilenc személyt szűrtek át; 551-et kizártunk, közülük 460 nem volt jogosult, és 91-en visszavonultak a szűrés során (1. ábra). A faj és az etnikai hovatartozás önjelölt volt.
Résztvevő áramlása a tárgyaláson.
Alapvonal
A teljes energiafelhasználást kétszer (kéthetes periódusok) mértük a kiindulási értéken, kétszeresen jelölt víz alkalmazásával, míg a résztvevők szokásos étrendjüket otthon követték (B1), máskor pedig testsúly-fenntartó étrendet kaptak (B2). Röviden, az alanyok adagolás előtt 2 vizeletmintát adtak be (2,0 g 10% dúsított H218O és 0,12 g 99,9% dúsított 2 H2O a becsült teljes testvíz kilogrammonként), és további időzített mintákat vettek 4,5, 6h és 7 és 14 nappal az adagolás után. A szén-dioxid-termelést és az energiafelhasználást a korábban leírt 28, 29 szerint számoltuk. A B2 után az alanyok 5 napos fekvőbeteg-tartózkodáson vettek részt (M0), ahol számos anyagcsere-tesztet végeztek. Az alanyok megismételték a fekvőbeteg-tartózkodást az M3 és az M6-nál.
Közbelépés
Nem és BMI szerinti rétegzés után az alanyokat (n = 48) 6 hónapon keresztül szekvenciálisan randomizáltuk a négy csoport egyikébe: Kontroll (testsúly-fenntartó étrend), CR = a kiindulási energiaigény kalória-korlátozása 25%, CREX = 12,5% CR + 12,5% -kal növekszik az energiafelhasználás strukturált testmozgással, LCD = nagyon alacsony kalóriatartalmú étrend, egészen 15% -os testsúlycsökkenésig, majd testsúly-fenntartó diéták. A beavatkozási csoport kivételével az adatgyűjtésben részt vevő összes személyzet elvakult a tantárgyi információktól, beleértve a kezelés kijelölését is.
Fogyókúrák
A kiindulási energiaigényt a mért EE alapján egyedileg számolták. Ezután minden alany számára menüt írtak fel a napi célbevitel 100 kcal-ján belül. A menüket Moore Extended Nutrient Database (MENu 2000, PBRC, Baton Rouge, LA) és ProNutra 3.0 (Viocare, Princeton, NJ) felhasználásával tervezték. A résztvevőket az összes táplálékkal ellátták a kiinduláskor (B2) és a randomizálást követő első 12 hétben. A résztvevők minden héten 2 ételt ettek a központban, 1 étkezéssel, valamint kivitelre csomagolt snackekkel. A résztvevők a 13-22. Héttől kezdve saját maguk választották ki diétájukat az egyes kalóriatartalmak alapján. A 22–24. Hétig visszatértek az etetési protokollhoz. Minden étrend (az LCD kivételével) az American Heart Association ajánlásain alapult (≤ 30% zsír). Az LCD résztvevőket 890 kcal/d-re (HealthOne, Health and Nutrition Technology, Carmel, Kalifornia) tettük fel 5 rázkódásként, amelyek napi 75 g fehérjét, 110 g szénhidrátot, 5 g zsírt és 10 g bolus zsírt tartalmaztak. A cél-fogyás (-15%) elérése után a résztvevőket lassan újratápláltuk egy olyan energiaszintre, amely fenntartotta a testtömeget. Általában a célsúlyt a férfiaknál a 8. hétig, a nőknél a 11. hétig érték el.
Viselkedési és testmozgási stratégiák
Az alanyok heti csoporttalálkozókon vettek részt, és a hét közepén telefonhívást kezdeményeztek az energiafogyasztás bejelentése érdekében, hogy a protokoll betartásával kapcsolatos problémákat gyorsan megoldják. Kognitív-viselkedési technikákat alkalmaztak az étrend és a testmozgás előírásainak betartásának elősegítésére, beleértve az önellenőrzést és az ingerkontrollt. A Health Management Resources Calorie System-t (HMR ™, Boston, MA) alkalmazták a résztvevők képzésére, hogy megbecsüljék az ételek kalóriatartalmát.
A CREX résztvevői az energiafelhasználást 12,5% -kal növelték a pihenésnél, strukturált testmozgáson (gyaloglás, futás, kerékpározás) hetente öt napon keresztül. A cél energiaköltség nőknél 403 (63) kcal volt, férfiaknál 569 (118) kcal. Az egyes testgyakorlati előírásokat az oxigénköltség (V-Max29 sorozat, SensorMedics, Yorba Linda, Kalifornia) mérésével számítottuk ki az előírt tevékenység három szintjén, és létrehoztunk egy egyenletet az energiafelhasználás becsléséhez. Az edzésenkénti átlagos testedzés időtartama nőknél 53 (11) perc, férfiaknál 45 (14) perc volt. A résztvevőknek heti 3 alkalmat kellett elvégezniük felügyelet mellett, és hordozható pulzusmérőket kellett viselniük (Polar S-610, Polar Beat, Port Washington, NY), hogy értékeljék a megfelelőséget a felügyelet nélküli ülések során.
Biokémiai elemzés
Az éhomi szérum inzulint, a DHEAS-t, a tiroxint (T4) és a tri-jod-tironint (T3) immunvizsgálatokkal (DPC 2000, Diagnostic Product Corporation, Los Angeles, CA) mértük. A glükózt glükóz-oxidáz elektróddal (Syncron CX7, Beckman, Brea, CA) elemeztük. A fehérjék karboniltartalmát módosított 2,4-dinitrofenilhidrazin (DNPH) vizsgálattal határoztuk meg Mates és mtsai 30 módszerével. .
Anyagcsere tesztek
DNS-fragmentáció egysejtes gélelektroforézissel (Comet assay)
Az üstökösvizsgálatot Deutsch és mtsai 34 szerint végeztük. Röviden, a teljes vérsejteket alacsony olvadáspontú agarózban szuszpendáltuk a kereskedelemben kapható tárgylemezeken (Trevigen, Gaithersburg, MD). A tárgylemezeket UV mikroszkóp alatt (Nikon Microphot FXA, Hamamatsu nagy felbontású 512 sor, Image I AT szoftver, FITC 3 szűrő) néztük meg. A DNS károsodás mértékét az üstökös farok pillanatának kiszámításával határoztuk meg, amely az üstökös farka integrált sűrűsége, szorozva a mag középpontjától a 25 sejt farka tömegközéppontjának távolságával, szabadon elérhető szoftverek segítségével (Herbert M Geller; http://www2.umdnj.edu/
geller/lab/üstökös-pontozás-makró.txt). Két egymást követő napon mért 20 egyénnél a módszer intraclass korrelációs együtthatója 0,95 volt.
Statisztikai analízis
A szövegben és a táblázatokban szereplő adatok eszközként (SEM) vannak megadva. Az elemzéshez a SAS 9.1 verziót használtuk. Az M3 és M6 változók változását a kiindulási értékhez képest ismételt mérésekkel elemeztük, a kezelés és az idő kölcsönhatásait, valamint a kiindulási értékeket kovariátként adva. A kiindulási lineáris regressziót (n = 48) használtuk az EE előrejelzésére szolgáló egyenletek előállításához, és a megjósolt értékeket a mért FFM egyenlet felhasználásával állítottuk elő. Az előrejelzett és a mért EE közötti különbségeket az ANOVA segítségével kiszámoltuk és elemeztük a fent leírtak szerint. Következtetésünk megerősítéséhez hasonló megközelítést alkalmaztunk prediktív egyenletek előállításához egy 865 nem cukorbeteg egyénből, egy hasonló anyagcsere-kamrában mérve 35. Normalizáló és varianciát stabilizáló logaritmikus transzformációt alkalmaztunk az üstökösvizsgálat számított faroknyomatékaira. A célminták 48-as nagysága biztosította a szükséges erőt az elsődleges végpont, az ülőenergia-ráfordítás 15% -os csökkenésének kimutatásához.
Eredmények
Két személy kivonult a vizsgálat befejezése előtt, egy a kontrollcsoportból a 4. héten (személyes okok) és egy az LCD csoportból az 5. héten (elveszítette a nyomon követést). Az alanyok pénzbeli kompenzációt kaptak a vizsgálat alatt és befejezése után. Ez, valamint az intervencióssal való gyakori kapcsolatfelvétel elősegítette a kiváló retenciós arányt.
Az értékeket eszközként (SEM) adjuk meg [tartomány].
C = kaukázusi, AA = afro-amerikai, O = egyéb
Az éhomi inzulin jelentősen csökkent a kiindulási értékhez képest az M3 és az M6 esetében a CR és CREX csoportokban (mindkettő, p 2. ábra), és az M6 esetén az összes csoportban (mindegyik, p 2. ábra). Az éhomi glükóz és a DHEAS egyik csoportban sem változott. A CR-re (-0,2 (0,05) ° C) és a CREX-re (-0,3 (0,08) ° C) randomizált alanyok átlagosan csökkentették a 24 órás testhőmérsékletet (mindkettő, p 3. ábra). Nem változott a maghőmérséklet a kontroll vagy az LCD csoportokban.
A súlycsökkenés százalékos aránya csoportonként. A kezdeti súlyt az alapvonal fázisában hetente mért 5 súly átlagaként regisztráltuk. Az időbeli súlyváltozás szignifikánsan különbözött a kontrollcsoport és a három intervenciós csoport között (p 2. táblázat). A kiinduláskor az FFM a mozgásszegény 24h-EE varianciájának 86% -át tette ki (24h-EE (kcal/d) = 596 + 26,8 * FFM, r 2 = 0,86, p 2. táblázat). Egyéni adatpontok az M6-on és az alapvonal regressziós vonala a 24h-EE vs. Az FFM-et a 4. ábra mutatja. Amikor a három beavatkozási csoportba tartozó alanyokat összevontuk, a korrigált 24 órás EE értékek statisztikailag alacsonyabbak voltak, mint az M3 és M6 kontrolloknál (35. o. csoportok a kiinduláskor vagy a kontrollok bármely időpontjában. Azonban a korrigált 24h-EE szignifikánsan alacsonyabb volt M3 és M6 esetén CR, CREX és LCD esetén (mindegyik p 2. táblázat és 4. ábra). a spontán fizikai aktivitás szintje és az étel termikus hatása az energiafogyasztás százalékában kifejezve.
A mag testhőmérsékletének változása a kiindulási értékről az M6-ra 23 óra alatt mérve egy metabolikus kamrában 22,2 (0,2) ° C-ra állítva.
Eszközök (SEM). Az előrejelzett EE-t * 24h-EE = 596 + 26,8 * FFM (r 2 = 0,86, p 2 = 0,76, p 2. ábra) módon számítottuk, csak időhatásra való hajlamot figyeltünk meg (p = 0,07). Hasonló eredményeket találtunk a plazma T4 változására a kezelésre adott válaszként (p 5. ábra). A DNS károsodása csökkent az alapvonaltól CR (-0,56 (0,11) au), CREX (-0,45 (0,12) au) és LCD (-0,35 (0,12) au) csoportokban az M6-on (mindez, p 5. ábra). Ez a csökkenés statisztikailag nem különbözött a kontrollaktól a három kezelési csoport kombinálásakor. Nem találtunk szignifikáns összefüggést a DNS károsodásának változásai és a beállított EE, FM vagy testtömeg változásai között.
Összefüggés a következők között: Felső panel: mért 24h-EE és zsírmentes tömeg. (24h-EE (kcal/d) = 596 + 26,8 * FFM, r 2 = 0,86, p 2 = 0,76, p 36, ismert, hogy a kalória-korlátozás (CR) meghosszabbítja az életet rágcsálókban és más alacsonyabb fajokban. Kevéssé ismert azonban a CR emberre gyakorolt hosszú távú hatása. Jelen tanulmányban megvizsgáltuk a 6 hónapos CR hatásait a CR biomarkereire, az energiafelhasználásra és az oxidatív stresszre emberben. Eredményeink azt mutatják, hogy az elhúzódó CR a következőket okozta: 1) a három korábban jelentett robusztus hosszú élettartamú biomarker (az éhomi éhomi inzulin és a test testhőmérséklete) megfordulása; 2) egy metabolikus adaptáció (az EE csökkenése nagyobb, mint a metabolikus tömeg csökkenése alapján várható volt), amely alacsonyabb pajzsmirigyhormon-koncentrációval társul, és 3) a DNS fragmentációjának csökkenése a DNS kevesebb károsodása következtében.
Számos CR biomarkert azonosítottak rágcsálókban, beleértve a hőmérsékletet, a DHEAS-t, a glükózt és az inzulint. Roth és mtsai. 26 nemrégiben megfigyelték, hogy a testhőmérséklet, az inzulin és a DHEAS a CR majmokban is megváltozott, igazolva azok biomarkerként való hasznosságát hosszabb életű fajokban. Fontos, hogy azt is megmutatták, hogy ezek a paraméterek megváltoztak a hosszabb életű férfiaknál. Ezek a megállapítások alátámasztják ezen tényezők szerepét az emberekben a hosszú élettartam biomarkereként. A főemlős modellhez hasonlóan a CR és CREX csoportokban szignifikánsan csökkent éhomi inzulin- és testmaghőmérsékletet figyeltünk meg. A DHEAS és az éhomi glükóz azonban nem változott beavatkozással. Valószínűleg ez a tanulmány nem volt elég hosszú ahhoz, hogy kimutassa a DHEAS változásokat, amelyek számítások szerint évente 2-4% -ot esnek az embereknél. Az éhomi glükózt a főemlősök hosszan tartó CR nem változtatja meg következetesen, ezért megkérdőjelezzük, hogy az éhomi glükóz hasznos-e biomarkerként a hosszabb életű fajokban. Másrészt Fontana és mtsai. 27 megfigyelte, hogy az éhgyomri glükóz és az inzulin jelentősen csökkent azoknál a CR-alanyoknál, akik 6 éve követték az ön által előírt táplálkozásilag megfelelő CR-diétákat.
E tanulmány eredményei azt mutatják, hogy a diéta vagy az étrend és a testmozgás kombinációjával történő elhúzódó CR sikeresen megvalósult, amit a csökkent testsúly, a zsírtömeg, az éhomi szérum inzulin és a test maghőmérséklete bizonyít. Ez a tanulmány egyedülálló abban az értelemben, hogy a kiindulási ponton gondosan megmérték az egyéni energiaigényt, amely lehetővé tette számunkra, hogy tápláljuk és felírjuk az egyes alanyok étrendi céljait. Megfigyeltük továbbá, hogy a „metabolikus alkalmazkodás” a nem elhízott emberek energiahiányára reagálva alakul ki 3 és 6 hónaposan, ami a zsírmentes tömeg egységére jutó oxigénfogyasztás csökkenését eredményezi, még a súlystabilitás elérése után is. Végül, ez a tanulmány megerősíti azokat a korábbi eredményeket, amelyek szerint a kalória korlátozás a DNS károsodásának csökkenését eredményezi. Hosszabb vizsgálatokra van azonban szükség annak megállapításához, hogy ezek a hatások fennmaradnak-e és befolyásolják-e az öregedési folyamatot.
- Korrekció Az intermittáló hatása a folyamatos energiakorlátozáshoz képest a fogyás és
- Teljes cikk A passzív melegítés hatása a 70-es hősokkfehérjére és az interleukin-6 A-ra lehetséges
- Túlsúly A váratlan fiúk pubertás hatása
- A terhesség korai súlygyarapodása a legerősebb hatást gyakorolja a születési súlyra, kritikus időt jelentve a
- Dyskinesia A Parkinson megértése; a Med Side Effect APDA-val