Foszfomicin
Jogi nyilatkozat
A WikiDoc NEM GARANTÁL AZ ÉRVÉNYESSÉGRŐL. A WikiDoc nem professzionális egészségügyi szolgáltató, és nem is alkalmas az engedéllyel rendelkező egészségügyi szolgáltató helyettesítésére. A WikiDoc oktatási eszköz, nem pedig az egészségügyi ellátás bármely formájának eszköze. A WikiDoc gyógyszeroldalakon az oktatási tartalom az FDA melléklete, az Országos Orvostudományi Könyvtár tartalma és gyakorlati irányelvei/konszenzusos nyilatkozatokon alapul. A WikiDoc nem támogatja olyan gyógyszerek vagy eszközök beadását, amelyek nem felelnek meg a címkézésének. Kérjük, olvassa el itt a teljes felelősségkizárásunkat .
Áttekintés
A fosfomicin egy antibakteriális szer, amelyet az FDA jóváhagyott a szövődmény nélküli húgyúti fertőzések kezelésére. A gyakori mellékhatások közé tartozik a hasmenés, hüvelygyulladás, émelygés, fejfájás, szédülés, aszténia, dyspepsia és az eozinofil- és fehérvérsejtszám emelkedése, bilirubin, ALT, AST, lúgos foszfatáz és a hematokrit, a hemoglobin és a vérlemezkék számának csökkenése.
Felnőttek javallatai és adagolása
FDA által jelzett indikációk és adagolás (felnőtt)
Komplikálatlan húgyúti fertőzések
- A foszfomicin csak komplikált húgyúti fertőzések (akut hólyaghurut) kezelésére javallt nőknél az Escherichia coli és az Enterococcus faecalis fogékony törzsei miatt. A foszfomicin nem javallt pyelonephritis vagy perinefricus tályog kezelésére.
- Ha a Fosfomycin-kezelés után a bakteriuria tartósan fennáll vagy újra megjelenik, más terápiás szereket kell választani.
Adagolási információk
- A komplikált húgyúti fertőzés (akut hólyaghurut) esetén a 18 éves vagy annál idősebb nők számára az ajánlott adag egy tasak Fosfomycin. A foszfomicint étkezés közben vagy anélkül is bevehetjük.
- A foszfomicint nem szabad száraz formában bevenni. Lenyelés előtt mindig keverje össze a Fosfomycint vízzel.
Címkén kívüli használat és adagolás (felnőtteknek)
Iránymutatással támogatott használat
A következőkkel kapcsolatban korlátozott információ áll rendelkezésre Címkén kívüli útmutató által támogatott használat felnőtt betegeknél.
Nem iránymutatással támogatott használat
A következőkkel kapcsolatban korlátozott információ áll rendelkezésre Címkén kívüli, nem iránymutatással támogatott használat felnőtt betegeknél.
Gyermekgyógyászati javallatok és adagolás
FDA által jelzett javallatok és adagolás (gyermek)
A 12 évesnél fiatalabb gyermekek biztonságosságát és hatékonyságát nem igazolták megfelelő és jól kontrollált vizsgálatokban.
Címkén kívüli használat és adagolás (gyermek)
Iránymutatással támogatott használat
A 12 évesnél fiatalabb gyermekek biztonságosságát és hatékonyságát nem igazolták megfelelő és jól kontrollált vizsgálatokban.
Nem iránymutatással támogatott használat
A 12 évesnél fiatalabb gyermekek biztonságosságát és hatékonyságát nem igazolták megfelelő és jól kontrollált vizsgálatokban.
Ellenjavallatok
- A foszfomicin ellenjavallt olyan betegeknél, akiknek ismert túlérzékenysége van a gyógyszerrel szemben.
Figyelmeztetések
- A Clostridium difficileassociated hasmenésről (CDAD) beszámoltak szinte minden antibakteriális szer, így a Fosfomycin alkalmazása esetén, és súlyossága az enyhe hasmenéstől a fatális vastagbélgyulladásig terjedhet. Az antibakteriális szerekkel végzett kezelés megváltoztatja a vastagbél normál flóráját, ami a C. difficile túlnövekedéséhez vezet.
- A C. difficile olyan A és B toxinokat termel, amelyek hozzájárulnak a CDAD kialakulásához. Hypertoxint termelő C törzsek. A difficile fokozott morbiditást és mortalitást okoz, mivel ezek a fertőzések refrakterek lehetnek az antimikrobiális terápiával szemben, és kolektómiát igényelhetnek. A CDAD-t figyelembe kell venni minden olyan betegnél, akinek hasmenése jelentkezik az antibiotikumok használatát követően. Gondos kórtörténetre van szükség, mivel a CDAD az antibakteriális szerek beadása után két hónapon belül jelentkezett.
- Ha a CDAD gyanúja merül fel vagy megerősítést nyer, a folyamatos antibiotikum-használat nem irányul a C ellen. a nehézségeket fel kell függeszteni. Megfelelő folyadék- és elektrolitkezelést, fehérje-kiegészítést, a C. difficile antibiotikum-kezelését és műtéti értékelést kell elvégezni, amint azt klinikailag indokolt.
Óvintézkedések
- Tábornok
- Az akut hólyaghurut egyetlen epizódjának kezelésére ne használjon egynél több Fosfomycin adagot.: * A Fosfomycin ismételt napi dózisa nem javította a klinikai sikert vagy a mikrobiológiai kiirtási arányt az egyszeri dózisú terápiához képest, de növelte a nemkívánatos események előfordulását. A tenyésztés és az érzékenység vizsgálatára szolgáló vizeletmintákat a terápia befejezése előtt és után kell beszerezni.
Mellékhatások
Klinikai vizsgálatok tapasztalatai
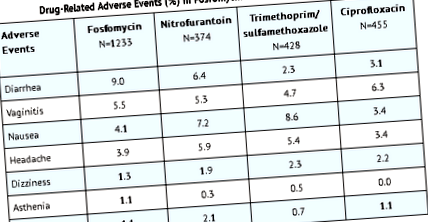
- Klinikai vizsgálatokban az alábbiakban felsoroljuk azokat a gyógyszerrel kapcsolatos mellékhatásokat, amelyekről a foszfomicinnel kezelt vizsgálati populáció több mint 1% -ánál számoltak be:
- A klinikai vizsgálatok során a leggyakrabban jelentett mellékhatások, amelyek a gyógyszerpopulációtól függetlenül a vizsgált populáció> 1% -ánál fordultak elő:
- Hasmenés 10,4%, fejfájás 10,3%, hüvelygyulladás 7,6%, émelygés 5,2%, nátha 4,5%, hátfájás 3,0%, dysmenorrhealis 2,6%, garatgyulladás 2,5%, szédülés 2,3%, hasi fájdalom 2,2%, fájdalom 2,2%, dyspepsia 1,8%, aszténia 1,7% és kiütés 1,4%.
- A klinikai vizsgálatokban a következő nemkívánatos események kevesebb, mint 1% -os arányban fordultak elő, függetlenül a gyógyszer kapcsolatától:
- Rendellenes széklet, étvágytalanság, székrekedés, szájszárazság, dysuria, fülzavar, láz, puffadás, influenza szindróma, hematuria, fertőzés, álmatlanság, lymphadenopathia, menstruációs rendellenesség, migrén, myalgia, idegesség, paresthesia, viszketés, fokozott SGPT, bőrzavar, aluszékonyság és hányás.
- Az egyik betegnél egyoldalú optikai ideggyulladás alakult ki, amely esemény valószínűleg a Fosfomycin terápiával függ össze.
Postmarketing tapasztalat
- Az Egyesült Államokon kívüli, a Fosfomycin-szel kapcsolatos marketing tapasztalatokból származó súlyos mellékhatásokról ritkán számoltak be, és ezek közé tartoznak: angioödéma, aplasticanemia, asztma (exacerbáció), kolesztatikus sárgaság, máj nekrózis és toxikus megakolon.
- Bár az okozati összefüggést nem sikerült megállapítani, a forgalomba hozatalt követő megfigyelés során a következő események fordultak elő a foszfomicint felírt betegeknél: anafilaxia és halláskárosodás.
Gyógyszerkölcsönhatások
- Metoklopramid
- A foszfomicinnel együtt adva a metoklopramid, amely a gyomor-bélrendszeri motilitást fokozza, csökkenti a foszfomicin szérumkoncentrációját és vizelettel történő kiválasztását. A gyomor-bél traktus motilitását növelő egyéb gyógyszerek hasonló hatásokat produkálhatnak.
- Cimetidin
- A cimetidin a foszfomicinnel együtt alkalmazva nem befolyásolja a foszfomicin farmakokinetikáját.
Használat meghatározott populációkban
Terhesség
Teratogén hatások
- A foszfomicin intramuszkulárisan, nátrium-só formájában, 1 g dózisban terhes nőknek átjut a placenta gáton. A foszfomicin átjut a patkányok placenta gátján; 1000 mg/kg/nap dózisban (kb. 9 és 1,4-szerese az emberi testtömeg és mg/m2-nek megfelelő dózis) vemhes patkányokban nem okoz teratogén hatást. Terhes nőstény nyulaknak napi 1000 mg/kg-os dózisban (az emberi dózis körülbelül 9, illetve 2,7-szerese a testtömegre, illetve mg/m2-re vonatkoztatva) fetotoxicitást figyeltek meg. Ezeket a toxicitásokat azonban anyai szempontból mérgező dózisoknál tapasztalták, és úgy vélték, hogy azok a nyúl érzékenységének tudhatók be az antibiotikum beadása következtében a bél mikroflóra változásaira. Terhes nőkön azonban nincs megfelelő és jól kontrollált vizsgálat. Mivel az állatszaporítási vizsgálatok nem mindig jósolják az emberi reakciót, ezt a gyógyszert terhesség alatt csak akkor szabad alkalmazni, ha egyértelműen szükséges.
- Ausztrál Gyógyszerértékelő Bizottság (ADEC) terhességi kategóriája
Nincs ausztrál gyógyszerértékelő bizottság (ADEC) útmutatása a foszfomicin terhes nőknél történő alkalmazásáról.
Munka és szállítás
Nincs FDA útmutatás a foszfomicin használatáról a vajúdás és a szülés során.
Szoptató anyák
- Nem ismert, hogy a foszfomicin-trometamin kiválasztódik-e az anyatejbe. Mivel sok gyógyszer kiválasztódik az anyatejbe, és mivel a szoptató csecsemőknél súlyos mellékhatások jelentkezhetnek a Fosfomycinből, döntést kell hozni az ápolás abbahagyásáról vagy a gyógyszer beadásának elmaradásáról, figyelembe véve a gyógyszer fontosságát az anya számára.
Gyermekgyógyászati felhasználás
- A 12 évesnél fiatalabb gyermekek biztonságosságát és hatékonyságát nem igazolták megfelelő és jól kontrollált vizsgálatokban.
Geriatikus használat
- A foszfomicin klinikai vizsgálatai nem tartalmaztak elegendő számú 65 éves vagy annál idősebb személyt annak eldöntésére, hogy másképp reagálnak-e, mint a fiatalabbak. Más beszámolt klinikai tapasztalat nem azonosított válaszreakciókat az idős és a fiatalabb betegek között. Általában az idős betegeknél az adag kiválasztásának óvatosnak kell lennie, általában az adagolási tartomány alsó végétől kezdődően, tükrözve a csökkent máj-, vese- vagy szívműködés, valamint az egyidejűleg előforduló betegség vagy más gyógyszeres kezelés gyakoriságát.
Nem
Nincsenek FDA útmutatások a foszfomicin alkalmazásáról a nemek specifikus populációi tekintetében.
Nincsenek FDA útmutatások a foszfomicin specifikus faji populációk tekintetében történő alkalmazásáról.
Vesekárosodás
Nincs FDA útmutatás a Fosfomycin vesekárosodásban szenvedő betegeknél történő alkalmazásáról.
Májkárosodás
Nincs FDA útmutatás a Fosfomycin májkárosodásban szenvedő betegeknél történő alkalmazásáról.
Szaporodási potenciállal rendelkező nők és férfiak
Nincs FDA útmutatás a foszfomicin reproduktív potenciállal rendelkező nőknél és férfiaknál történő alkalmazásáról.
Immunhiányos betegek
Nincs FDA útmutatás a Fosfomycin alkalmazásáról immunhiányos betegeknél.
Adminisztráció és ellenőrzés
Adminisztráció
Monitoring
A következőkkel kapcsolatban korlátozott információ áll rendelkezésre Monitoring foszfomicin a gyógyszer címkéjén
IV Kompatibilitás
A következőkkel kapcsolatban korlátozott információ áll rendelkezésre IV Kompatibilitás foszfomicin a gyógyszer címkéjén.
Túladagolás
- Akut toxikológiai vizsgálatokban nagy, legfeljebb 5 g/kg foszfomicin dózisok szájon át történő beadása egerekben és patkányokban jól tolerálható volt, nyulaknál átmeneti és kisebb mértékű vizes székletet okozott, kutyáknál pedig 2-3 napos anorexiás hasmenést okozott. egyszeri adagolás után. Ezek az adagok az emberi terápiás dózis 50-125-szeresét jelentik.
- A következő eseményeket figyelték meg olyan betegeknél, akik túladagolásban szedték a Fosfomycint: vestibularis veszteség, halláskárosodás, fémes íz és az ízérzékelés általános csökkenése. Túladagolás esetén a kezelésnek tüneti és támogatónak kell lennie.
Gyógyszertan
A cselekvés mechanizmusa
- A foszfomicin (a foszfomicin-trometamin aktív komponense) in vitro aktivitást mutat a gram-pozitív és gram-negatív aerob mikroorganizmusok széles skálájával szemben, amelyek szövődmény nélküli húgyúti fertőzésekkel társulnak. A foszfomicin terápiás dózisban baktériumölő hatású a vizeletben. A foszfomicin baktericid hatása az enolpiruvil-transzferáz enzim inaktiválásának köszönhető, és ezzel visszafordíthatatlanul blokkolja az uridin-difoszfát-N-acetil-glükózamin kondenzációját p-enol-piruváttal, amely a bakteriális sejtfal szintézisének egyik első lépése. Csökkenti a baktériumok ragaszkodását az uroepithelialis sejtekhez is.
- Általában nincs keresztrezisztencia a foszfomicin és más típusú antibakteriális szerek, például béta-laktámok és aminoglikozidok között.
- A foszfomicinről kimutatták, hogy aktív a következő mikroorganizmusok legtöbb törzse ellen, mind in vitro, mind klinikai fertőzésekben
- Aerob gram-pozitív mikroorganizmusok
- Enterococcus faecalis
- Aerob gram-negatív mikroorganizmusok
- Escherichia coli
Szerkezet
- A foszfomicin (foszfomicin-trometamin) tasak foszfomicin-trometamint tartalmaz, szintetikus, széles spektrumú, baktericid antibiotikum orális alkalmazásra. Egydózisos tasakként kapható, amely fehér szemcséket tartalmaz, amelyek 5631 gramm foszfomicin-trometaminból (3 gramm foszfomicinnek felel meg) és a következő inaktív összetevőkből állnak: mandarin aroma, narancs aroma, szacharin és szacharóz. A tasak tartalmát fel kell oldani vízben. A foszfomicin-trometamin, egy foszfonsav-származék, (1R, 2S) - (1,2-epoxi-propil) -foszfonsavként kapható, amely vegyület 2-amino-2- (hidroxi-metil) -1,3-propándiollal (1: 1) tartalmaz. . Ez egy fehér szemcsés vegyület, amelynek molekulatömege 259,2. Empirikus képlete C3H7O4P.C4H11NO3, kémiai szerkezete a következő:
Farmakodinamika
A következőkkel kapcsolatban korlátozott információ áll rendelkezésre Farmakodinamika foszfomicin a gyógyszer címkéjén.
- Fosfomycin Michigan Medicine
- Széklet okkult vér - wikidoc
- Farmina Kisállateledelek - Kutyaeledel - Farmina Vet Life szemfogak - Vese nedves táplálék szemfogak
- Távollátás Okok és korrekciós kezelések
- A megélhetési költségek meghatározzák, hogy a bálnák, delfinek és a delfinek mit esznek a zsákmányminőség fontosságán