Hijamat (nedves köpölyözés) hatékonysága alkoholmentes zsírmájbetegségben szenvedő iráni betegeknél: kontrollált klinikai vizsgálat
Homayoon BASHIRI
1 Fertőző betegségek kutatóközpontja, Kermanshah Orvostudományi Egyetem, Kermanshah, Irán,
2 Belgyógyászati Klinika, Kermanshah Orvostudományi Egyetem, Kermanshah, Irán,
Arezoo BOZORGOMID
1 Fertőző betegségek kutatóközpontja, Kermanshah Orvostudományi Egyetem, Kermanshah, Irán,
Vahid SHOJAEIMOTLAGH
3 Orvosi sebészeti osztály, Khoy Orvostudományi Egyetem, Khoy, Irán,
A szerzők kijelentik, hogy nincsenek összeférhetetlenségük.
Absztrakt
Háttér/cél
A nem alkoholos zsírmájbetegség (NAFLD) a világon a legelterjedtebb krónikus májbetegség. Ennek a betegségnek az előfordulása drámai módon megnőtt az elmúlt évtizedben. A vizsgálatok kimutatták, hogy szoros kapcsolat van a ferritin szintje és a NAFLD súlyossága között. Jelen tanulmány célja annak értékelése volt, hogy a Hijamat, mint vas-redukáló eljárás, hogyan adható hozzá a szokásos életmód-módosításhoz az inzulinrezisztencia és a májenzimek javulására a NAFLD-ben szenvedő betegeknél.
Anyagok és metódusok
Százhúsz NAFLD beteg vett részt a vizsgálat randomizált, kontrollált, egyszeres vak vizsgálatban. A kontrollcsoport táplálkozással és fizikai aktivitással kapcsolatos tanácsokat kapott 6 hónapig. A kezelőcsoport 1 hónap alatt 3 alkalommal kapta meg a fenti elemeket, valamint a Hidzsátot. A máj ultrahangos képeit, a HOMA-IR-t és a laboratóriumi adatokat, beleértve az ALT-t, az AST-t is, értékelték a beavatkozás előtt és után.
Eredmények
A vizsgálat végén a HOMA-IR szérumszintjének szignifikáns csökkenését mutattuk ki (–1,30 ± 0,88 vs –,02 ± 0,47, P Kulcsszavak: Alkoholmentes zsírmájbetegség, nedves köpölyözés, Hiamat, ALT, AST
1. Bemutatkozás
A nem alkoholos zsírmájbetegség (NAFLD) a betegségek spektrumát képviseli, a steatosistól a steatohepatitisig, a fibrózisig, a cirrhosistól, sőt a hepatocellularis carcinomáig, amelyet a hepatocitákon belüli lipidfelhalmozódás jellemez [1]. A NAFLD előfordulása az elmúlt 3 évtizedben növekszik, világszerte elérve a 6–35% -ot a felnőtt lakosság körében [2]. Ennek a magas gyakoriságnak az egyik legfontosabb oka a mozgásszegény életmód és a modern táplálkozási szokások globalizációja, a központi (hasi) elhízás, a 2-es típusú diabetes mellitus, a dyslipidaemia és a metabolikus szindróma fokozott előfordulása mellett [3].
Noha a NAFLD patogenezisében szerepet játszó molekuláris mechanizmusok még mindig kevéssé ismertek, az inzulinrezisztencia hozzájárul a szabad zsírsavak fokozottabb májba juttatásához és a máj lipidjeinek túltermeléséhez, ami végül a NAFLD-hez vezet [4]. Különböző vizsgálatok szerint a szérum ferritin magas szintje, mint a vasraktározás szokásos markere, a szabad gyökök növekedésével jár és inzulinrezisztenciát vált ki a myocytákban, a zsírszövetben [5].
A nedves köpölyözés vagy hidzsamát az egyik legrégebbi orvosi technika Ázsiában, a Közel-Keleten és Európában. Széles körben hivatkoznak az iráni hagyományos orvoslás dokumentumaira a különféle rendellenességek megelőzésére és kezelésére [6]. Ebben az eljárásban az okozati kóros anyagok kiválasztódnak a bőr kapilláris hálózatában található interstitialis id uidból és a vérből a szívás és a hegesedés lépései után [7]. Néhány tanulmány szerint a vas flebotómiával történő eltávolítása javítja az inzulinrezisztenciát és a májenzimeket a normális szérum ferritin- és transzferrinszinttel rendelkező NAFLD-betegeknél [8,9]. Hidzsátattól eltérően a test egyik felszínes vénáját szikével vágják le, és phlebotomiában kis mennyiségű vért távolítanak el a testből [10]. A legtöbb ember általában a hidzsamát részesíti előnyben a phlebotomia helyett, mert ez könnyebb és kevesebb fájdalmat okoz. A szérum ferritin és a NAFLD közötti kapcsolat kumulatív bizonyítékainak fényében ezt a vizsgálatot a Hijamat-terápia szerepének értékelésére végezték a májenzimek és a HOMA-IR javulásában NAFLD-ben szenvedő betegeknél.
2. Anyagok és módszerek
2.1. Dizájnt tanulni
A vizsgálat randomizált, egyszeres (megfigyelő-vak) vizsgálat volt, és a vizsgálat időtartama 6 hónap volt. A tanulmány tervét az ábra szemlélteti. A pácienseket véletlenszerűen felosztottuk a kezelési és a kontroll csoportokra, a számítógépes rétegzett blokkolt randomizálási módszer alkalmazásával. Az összes NAFLD-eset kezdetben rutinkezelésként tanácsot kapott a szénhidrát, vörös hús, sült ételek, cukrok és zsír bevitelének csökkentésére, valamint a rostbevitel és a testmozgás növelésére (legalább 20 perc, hetente háromszor). 4 hónap elteltével a kezelõcsoport 1 hónap alatt 3 alkalommal kapott hidzsamát (0 nap, 14 nap és 28 nap) [11]. Hidzsamát steril, eldobható csészékkel végeztünk 5 ponton: mindkét lapocka, ágyéki régió és csúcs. Ezekre a pontokra eldobható poharakat helyeztek, és köpölyözéses pumpával negatív nyomást alkalmaztak. Körülbelül 2-3 perc elteltével a csészéket eltávolítottuk. Ezután 26 mm-es eldobható lándzsákat használtunk 2 mm mélységig skarifikáláshoz a csészék helyén. A vákuumszivattyúzást másodszor is megismételték, és 3–5 cm3 véres ürítést távolítottak el köpölyözésenként. A helyeket ezután steril betétekkel borítottuk be.
2.2. A vizsgálat résztvevői
Az alanyokat 18 éves vagy annál idősebb felnőttek közül választottuk ki, akik sorra utaztak az Imam Reza Terápiás Oktatási Kórház (Kermanshah, Irán) Gasztroenterológiai és Hepatológiai Klinikájára, a NAFLD diagnózisával. Ez a kórház a legnagyobb központ az Irántól nyugatra fekvő Kermanshah tartományban. A NAFLD diagnózisát klinikai bizonyítékok, májenzimek és ultrahangvizsgálati kritériumok alapján állapították meg. Valamennyi alany megalapozott írásbeli beleegyezést adott a tanulmányhoz. A vírusos hepatitis B és/vagy C fertőzésben, sárgaságban, autoimmun hepatitisben, Wilson-kórban, α-1-antitripszin hiányban, cukorbetegség 1. típusú vagy másodlagos formáiban, coeliakia, alkoholfogyasztás, kortikoszteroidok fogyasztása és vesebetegségek, valamint terhes betegek vagy szoptató nőket kizárták a vizsgálatból. A szűrés során a beteginterjúkból olyan demográfiai adatokat gyűjtöttek, mint az életkor, a nem és a kórtörténet.
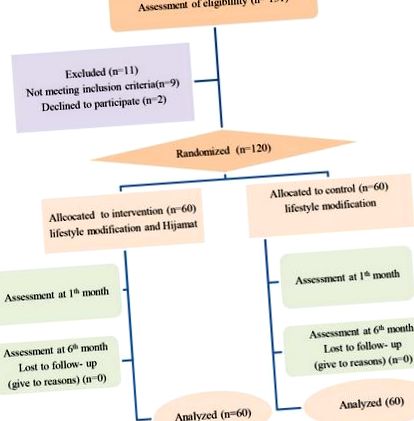
Folyamatábra ennek a klinikai vizsgálatnak az elosztásáról, nyomon követéséről és elemzéséről.
2.3. Minta nagysága
Nem voltak hasonló vizsgálatok, amelyek a minta nagyságának vizsgálatában segítettek volna minket. Javasolták, hogy körülbelül 60 beteg legyen ésszerű mintaméret a kísérleti vizsgálat során a kezelési hatások vizsgálatára [12]. Ezért úgy döntöttünk, hogy minden csoportba legalább 60 beteget toborozunk kényelmi mintaként.
2.4. Biokémiai értékelés
Vérmintákat vettünk a résztvevőktől egy 12 órás éjszakai böjt után a beavatkozás előtt és után. A szérum elválasztása után a mintákat jelöltük és –70 ° C-on tároltuk az elemzésig. Az alanin-aminotranszferáz (ALT) és az aszpartát-aminotranszferáz (AST) enzimatikus aktivitását a Hitachi 902 autoanalizátorral (Japán) mértük Pars Azmoon (iráni) analitikai készletek felhasználásával. Az ALT és az AST laboratóriumi referencia tartománya 5-41 NE/L, illetve 5-37 NE/L volt. Az inzulinrezisztenciát a homeosztázis modell értékelésével (HOMA-IR) határoztuk meg az alábbi képlettel: éhomi inzulin (µu/ml) × éhomi glükóz (mmoL/dL)/405.
2.5. A máj ultrahangos képalkotása
Az egyes résztvevők ultrahangos képeit is értékelték a beavatkozás előtt és után. A máj steatosisát 0-nak (zsír felhalmozódása nélkül), 1-nek (az echogenicitás minimális növekedése a rekeszizom és a portális vénafal normális megjelenése mellett), 2-nek (az echogenicitás mérsékelt növekedése, valamint a portális véna falának és a rekeszizomnak kissé károsodott megjelenítésével) osztályozták és 3 (az echogenicitás súlyos növekedése a diafragma, a portális véna falának és a jobb májlebeny hátsó részének rossz vagy nem látható megjelenítésével együtt) [13].
2.6. Statisztikai analízis
Az SPSS szoftvert használtuk a statisztikai elemzés 16. verziójához (SPSS Inc., Chicago, IL, USA). A Kolmogorov - Smirnov tesztet alkalmaztuk az adatok normális eloszlásának értékelésére az egyes csoportokban. A folyamatos változókat átlag ± szórásként (SD) mutatjuk be. Független minták t-tesztjét vagy Mann - Whitney U-tesztet alkalmaztuk a csoportok közötti összehasonlításhoz, és páros t-tesztet alkalmaztunk a csoporton belüli összehasonlításokhoz. A kategorikus változókat chi-square teszt segítségével hasonlítottuk össze. A P 0,05), így a csoportok összehasonlíthatók voltak. A betegek jellemzőit az 1. táblázat ismerteti.
Asztal 1
A kontroll és a hidzsamát csoportok alapjellemzői és biokémiai paraméterei.
| Kor, évek | 40,53 ± 7,32 | 38,38 ± 9,26 | 0,161 a |
| Neme, nő (%) | 29. (48.33) | 30 (50) | 0,855 b |
| ALT, NE/L | 46,30 ± 4,26 | 45,88 ± 4,39 | 0,883 c |
| AST, NE/L | 45,46 ± 5,25 | 44,33 ± 4,79 | 0,220 a |
| HOMA-IR | 2,23 ± 0,62 | 3,19 ± 0,65 | 0,630 c |
| Szonográfia (%) | |||
| I. fokozat | 26. (43.3) | 31. (51.7) | 0,364 b |
| Évfolyam II | 34. (56.7) | 28. (46.7) | |
| Évfolyam III | - | 1. (1.7) |
Az értékeket átlag ± SD-ként fejezzük ki
független minta t-teszt
b Khi-négyzet teszt
c Mann - Whitney U teszt
- Bél mikrobiota és alkoholmentes zsírmájbetegség - ScienceDirect
- Hipokalorikus étrend hatása transzaminázokban alkoholmentes zsírmájbetegségben és elhízott
- Zsíros májbetegség egy csendes gyilkos Narayana Health
- A zsírmáj betegség növekszik - Szórakozás és élet - Stroudsburg, PA
- ZSÍROS MÁJBETEGSÉG