Szövet átlátszósága in vivo
Mihail Injusin
1 Élettani Tanszék, Közép-Karibi Egyetem, Bayamon, PR 00960, USA
Daria Meshalkina
2 Szecsenov Evolúciós Élettani és Biokémiai Intézet, St. Petersburg 194064, Oroszország
Lidia Zueva
1 Élettani Tanszék, Közép-Karibi Egyetem, Bayamon, PR 00960, USA
Astrid Zayas-Santiago
1 Élettani Tanszék, Közép-Karibi Egyetem, Bayamon, PR 00960, USA
Absztrakt
Az in vivo szövet átlátszósága a látható fény spektrumában számos olyan optikai módszert alkalmazó kutatási alkalmazás számára előnyös, függetlenül attól, hogy magában foglalja-e a sejtek vagy azok aktivitásának in vivo optikai képalkotását, vagy optikai beavatkozást, hogy befolyásolja a sejteket vagy azok mélyen a szövetek belsejében, például az agyszövetben . A klasszikus nézet szerint egy szövet átlátszó, ha nem szívja el és nem szórja el a fényt, és így az abszorpció és a szóródás a legfontosabb elem, amelyet ellenőrizni kell a szükséges átlátszóság eléréséhez. Ez az áttekintés a legújabb fény- és kémiai megközelítésekre összpontosít a szöveti pigmentek színtelenítéséhez a látható fényelnyelés csökkentése érdekében, valamint az élő szövetekben történő szóródás csökkentésére szolgáló módszerekre. Megbeszéljük az átláthatóság lehetséges molekuláit is.
1. Bemutatkozás
Sok állat átlátszó szövetekkel rendelkezik, vagy teljesen átlátszóak a mindennapi életben. Egyesek tetszés szerint akár teljesen átlátszóvá is válhatnak, például bizonyos lábasfejű puhatestűek, amelyek megváltoztatják bőrük fényadszorpcióját (Zylinski és Johnsen, 2011) [1], a képi mélység jelzéseitől és az irányított megvilágítástól függően (Zylinski et al., 2016) [ 2]. A természetes átlátszósággal rendelkező állatok jelentős előnyökkel járnak a kutatás szempontjából, kiterjesztve a különböző optikai módszerek alkalmazásának lehetőségeit (Fetcho és O'Malley, 1995; O'Malley és mtsai, 2003; White és mtsai, 2008; Bin és Lyons, 2016; Antinucci és Hindges, 2016; Harrison és mtsai, 2016; Nicolson, 2017; Saleem és Kannan, 2018) [3,4,5,6,7,8,9,10]. Még akkor is, ha az állat általában nem átlátszó, általában speciális, átlátszó sejtekkel rendelkezik, legalábbis az állat vizuális rendszerében, és ez a sejtek átláthatósága konkrétan elemezhető (Zayas et al., 2018) [11]. Felmerülnek kérdések: Miért vannak az élő sejtek átlátszók, míg mások nem? Fenntarthatjuk-e az élő sejteket, miközben technikai célokra in vivo átlátszóvá teszjük őket? Átláthatóvá vagy legalább részben átlátszóvá tehetjük-e az állatokat, vagy fejleszthetünk-e in vivo átlátszó állati szöveteket és szerveket?
A klasszikus nézet szerint egy szövet átlátszó, ha nem szívja el és nem szórja el a fényt. Így az abszorpció és a szétszóródás a legfontosabb elem, amelyet ellenőrizni kell a szükséges szöveti átlátszóság elérése érdekében.
Néhány pigment kivételével a sejtben található szerves molekulák többsége nem képes elnyelni a látható fényt. Így ezeknek a pigmenteknek az (1) eliminálása csökkenti az abszorpciót és ezáltal elszíneződést eredményez. Ez kémiailag elérhető reaktív anyagok hozzáadásával, amelyek megszüntetik a specifikus pigmenteket, vagy genetikailag specifikus mutációk azonosításával, amelyek megzavarják a pigment bioszintézisét. A pigmentek eltávolítása után a szerves szövetek fennmaradó opálosságának elsődleges oka a fényszóródás (Brunsting és Mullaney, 1974; Tardieu és Delaye, 1988) [12,13].
2. Módszerek a fényelnyelés csökkentésére
2.1. A pigmentek kémiai színezése
2.2. A pigmentek eltávolításának genetikai megközelítése
3. Módszerek a fényszórás csökkentésére
3.1. A szórás kémiai csökkentése in vivo
3.2. Genetikai megközelítés a szórás csökkentésére
Mint már említettük, a citoplazma és a sejtes organellumok, valamint a sejtek és az intersticiális folyadék között RI-eltérés van, amely az élő szövetek által optikai szórást eredményez, és a citoplazmába juttatott OCA csökkentheti ezt az eltérést. Ahelyett, hogy külső szintetikus OCA-t juttatna a szövetbe, maga a sejt szintetizálhatja. Felmerül a kérdés: Milyen endogén OCA-kat használnak a természetben az állati szövetek átlátszóvá tételéhez (például a szem átlátszó szövetéhez), és hogyan tudjuk genetikailag manipulálni és koncentrálni ezt az anyagot a sejtben? Jelenleg a publikált tanulmányok többsége megpróbálta először azonosítani a természetes OCA-t és a hozzá tartozó szintézis géneket, hogy genetikai megközelítést lehessen alkalmazni, és az endogén OCA-k két fő molekuláris osztályát azonosították.
3.2.1. Glikozaminoglikánok és fagyálló fehérjék a halakban
3.2.2. Kristályok
A gerinces optikai traktus sejtjei túlnyomóan átlátszók. A kristályoknak nevezett specifikus kis molekulatömegű oldható fehérjék (a kristálylencse miatt) a gerinces optikai traktus számos sejtjének citoplazmájában különösen nagy mennyiségben találhatók. Nagy mennyiségű kristályt fedeztek fel a szaruhártya sejtek citoplazmájában, mind a szaruhártya hámsejtjeiben, mind a sztrómás keratocitákban (Krishnan et al., 2007; Jester, 2008) [69,70]. Hasonlóképpen, a kristályok bőségesen megtalálhatók a gerinces lencsében lévő, nagyon hosszúkás rostos sejtek citoplazmájában és a lencse hámsejtjeiben (Delaye és Tardieu, 1983; Horwitz és mtsai, 1999; Andley és mtsai, 2009) [71,72,73] . A retinában 23 kDa molekulatömegű (mind az αA-, mind az αB-kristályinnak megfelelő) kristályokat írtak le a béka (anuran) Müller sejtekben (Simirskiĭ et al., 2003) [74], és találtunk αA-kristálytint. egerek és patkányok fotoreceptor sejtjeiben (Deretic et al., 1994; Maeda et al., 1999) [75,76]. Nemrégiben a patkány Muller-sejtekben és a fotoreceptorokban kristályos α-t és specifikusan αA-kristályint írtunk le (Zayas-Santiago et al., 2018) [11].
Kimutatták, hogy a kristályok mind a szaruhártyában, mind a lencsében fontosak a sejtek átláthatósága szempontjából (Delaye és Tardieu, 1983; Takemoto, Boyle, 1998; Jester, 2008) [70,71,77]. A kristályok kémiai vagy genetikai módosulása átlátszatlansághoz, míg az oldható α-kristályok redukálása szürkehályoghoz vezet (Datiles et al., 2008) [78]. Hasonlóképpen, a szaruhártyában a szaruhártya kristályainak csökkent expressziója a sztrómás keratocitákban összefüggésbe hozható az in vitro és az in vivo fényszóródások fokozásával (Jester, 2008) [70]. A lencsében pontmutációkat azonosítottak az α-, β- és γ-kristályokat kódoló génekben, amelyek az emberi szürkehályog örökletes formájának kialakulásához vezetnek, akár születéskor, akár korán kialakulva (Graw, 2009 Andley és mtsai, 2009) [73.79].
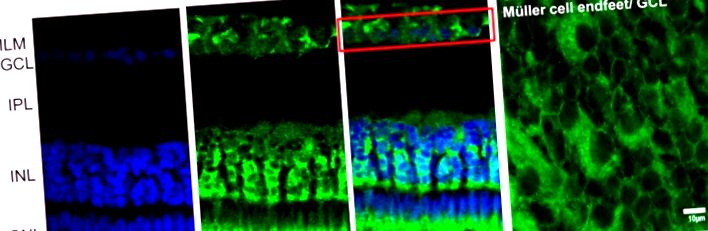
Az αA-kristályin immunolokalizálása a kajmán retinában. (A) Az αA-kristályin (CRYS, zöld) az idegsejteket körülvevő belső magrétegben (INL) expresszálódik (DAPI magfestés, kék). A kristályin szintén lokalizálódik a ganglion sejtmagok (vörös doboz) körül a ganglion sejtrétegben és a fotoreceptorok belső szegmensének területén. (B) A teljes retina szövet tetejéről megfigyelt αA-kristályzin. A kristály a Müller-sejtek végtagjaira korlátozódik a ganglion sejtrétegben (fehér nyíl). IPL, belső plexiform réteg; ILM, belső korlátozó membrán; GCL, ganglion sejtréteg; INL, belső magréteg; ONL, külső magréteg; IS, a fotoreceptorok belső szegmensei. Méretarány A-ban, 20 μm és B-ben, 10 μm.
Az αA-kristályin részvétele az átlátszóságban mikroorganizmusokban is igazolható. Ismert, hogy a Mycobacteriumnak lehet átlátszó (álló) vagy átlátszatlan (növekvő) fázisú sejttípusa, amely mutáció nélkül áttérhet egyikről a másikra, és ez az átmenet hőmérséklet-érzékeny. Az átlátszó változat tolerálja a magasabb növekedési hőmérsékleteket és ellenáll a legtöbb terápiás szernek. Mivel lehetséges, hogy az átlátszó variáns a betegség kórokozója az emberben, fontos megérteni az átlátszó-átlátszatlan átmenet mechanizmusát (Woodley, David, 1976) [89]. Az αA-kristályok egyszerre hősokk-fehérjék, lehetővé téve a sejtek túlélését magasabb hőmérsékleten, és átlátszóságot elősegítő szerek, és lehetséges, hogy a kristályok az átlátszó-átlátszatlan átmenet oka. Ismert, hogy a Mycobacteriumban található 16 kDa-os α-kristályos homológ az állófázisú tenyészetek által in vitro termelt domináns fehérje, de logaritmikusan növekvő kultúrákban nem mutatható ki (Yuan és mtsai, 1998; Stewart és mtsai, 2006). . [90.91].
3.2.3. Lehetséges genetikai manipuláció az átláthatóság és a jövőbeni perspektívák kiváltására
A glikozaminoglikánok géntechnológiával manipulált OCA-ként történő alkalmazása nehézkes, hatásukat nem teljesen ismerik. Másrészt az αA-kristályzin és kódoló génje jól jellemezhető. Bár ebben az irányban jelenleg nincs aktív fejlődés, azt javasoljuk, hogy a genetikai megközelítésnek ígéretes jövője legyen.
Az egyik nehézség az, hogy a kristályosoknak más funkcióik vannak a szervezetben, például hősokk-fehérjékként és szabályozó fehérjékként szolgálnak, és a túlzott expressziójukat az időzítés, az intenzitás és a szövet-specifitás szempontjából optimalizálni kell a szervezet fejlődésében és teljesítményében bekövetkező zavarok minimalizálása érdekében. A túlexpressziós megközelítés hosszú múltra tekint vissza a transzgenikus állatokban, mivel a célgén további kópiáinak túlexpressziója, amelyet tetraciklinre reagáló promóter ellenőrzése alatt vagy a Cas9 transzaktivátor expressziójával tartanak fenn. A fiziológiailag legmegfelelőbb változatnak a feltételes túlzott expressziót tekintjük, amely csak az induktor jelenlétében megy végbe, és nem zavarja a normális fejlődést. Így a mutált állatok normálisan fejlődnek, az átlátszóságot csak a kísérlet előtt indukálják, és az átlátszóság mértéke minden esetre optimalizálható.
A génexpresszió transzaktiválása a CRISPR-Cas9 génszerkesztő rendszer képessége (Perez-Pinera et al., 2013) [92]. Használja az inaktivált („elhalt”) Cas9 fúzióját (amely csak RNS-vezetőjével képes komplexet képezni és a célhoz kötődni, de nem képes levágni a célpontot) és egy transzkripciós aktivációs domén fúzióját, amelyet általában egy vírusból vesznek gén. Ennek a megközelítésnek az az előnye, hogy kifejezi az állat endogén génjét, amelynek szintjét a gén expressziójának alapszintje határozza meg, és Cas9-szel egyesített aktivációs domének hozzáadásával szabályozható (Cheng et al., 2013) [93].
Egy kísérleti szervezet, amely erre a megközelítésre alkalmazható, a zebrafish, amely már lárva formájában is átlátszó, de a felnőtteknél a fényszóródás miatt hiányzik a szükséges átláthatóság. Ezért a felnőttkori zebrafish-ban a kristály átlátszóságának kiváltása két stratégiával érhető el: (1) a kristálygének beépítése a tetraciklinre reagáló promóterek irányítása alá és (2) a transzaktivátor Cas9 gén beépítése több génnel az egyszeri vezető RNS-ek (sgRNS-ek). Mindkét megközelítésnek megvannak a benne rejlő előnyei és hátrányai, amelyek akadályt képezhetnek a stabil sejtvonal-generáció előtt. Sőt, ez a munka lehetővé teszi e megközelítések összehasonlítását, ami módszertanilag is értékessé teszi.
4. A csontok és más ásványi szövetek in vivo átlátszósága
5. Az átlátszóság egyéb modelljei
6. Következtetések
Sok kutató olyan módszereket dolgozott ki, amelyek kihasználják az in vivo szöveti transzparencia előnyeit. A hagyományos in vivo képalkotás és spektroszkópia, az optikai idegaktivitás rögzítése és stimulálása, valamint az optogenetika mind részesült a megnövekedett képmélységben, az in vivo optikai szövettisztítás különböző módszereivel. Két fő megközelítés létezik, kémiai (farmakológiai) és genetikai, amelyek csökkentik a fényelnyelődést és a szóródást egyaránt. Mindkét megközelítés erejét bebizonyították, de a mesterséges OCA-k káros hatásainak teljes kiküszöbölése érdekében azt javasoljuk, hogy az átlátszó szövetekkel rendelkező modell organizmusok előállításához szükséges genetikai módosítás az in vivo képalkotás jövőjét képviselje.
Szerző közreműködései
A felülvizsgálat szerzői szakterületük szerint írásban vettek részt: L.Z. és A.Z.-S. - mikroszkópia, D.M. - genetika, M.I. - képalkotás.
Finanszírozás
Ezt a kutatást a NIGMS (NIH) finanszírozta, az SC2GM111149 számú támogatás az MI számára.
Összeférhetetlenség
A szerzők nem jelentenek összeférhetetlenséget. A finanszírozóknak nem volt szerepük a tanulmány megtervezésében; az adatok gyűjtésében, elemzésében vagy értelmezésében; a kézirat írásában, vagy az eredmények közzétételéről szóló határozatban.
- Mi a lágy szöveti közelítés (TORe) és a WLS-kapcsolat; Súly Vissza az elhízásSúgó
- A szöveti faktor a visszatérő vénás tromboembólia előrejelzőjeként a rosszindulatú daganatok biomarker-elemzéseiben
- Szövetbővítő St.
- A jo-jo diéta újraelosztja a toxinokat a testszövetben; Az Olestra Plus kalóriavágás fokozza a mérgező kiválasztást -
- Szöveti sók - A Nature csodája mikrotápanyagok és hogyan kell használni őket! - Feelgood Health